Exercices Contrôle de la qualité par dosage
Prépare-toi à progresser en Physique-chimie avec ces exercices niveau Terminale : "Contrôle de la qualité par dosage". Conçu pour renforcer les notions clés vues en cours, cet entraînement te permet de t’exercer à ton rythme. Idéal pour réviser efficacement et gagner en confiance. À toi de jouer !
Entrainement
On effectue un dosage direct par conductimétrie de $100\ \text{mL}$ d’une solution aqueuse d’acide chlorhydrique. Pour cela, l’acide chlorhydrique $(\text{HCl})$ est dosé par une solution de soude $(\text{NaOH})$ de concentration $0,1\ \text{mol} \cdot \text{L}^{-1}$. Le montage d’un dosage par conductimétrie est mis en place incluant un conductimètre étalonné. La courbe obtenue admet un minimum pour un volume $V=12,5\ \text{mL}$.
Nous considérons que les conductivités molaires ioniques des ions $\text{CL}^-$ et $\text{Na}^+$ sont négligeables devant celles des ions $\text {H}_3\text{O}^+$ et $\text{HO}^-$.
Dans ce montage du dosage direct, quelle solution est placée dans la burette et laquelle est placée dans le bécher ?
Pour préparer un TP des terminales, Mme Erlen veut préparer une courbe étalon du dosage du permanganate de potassium $(\text K \text M \text N \text O_4)$ de couleur violette.
Dans un premier temps, Mme Erlen commence par mesurer l’absorbance $A$ de différents échantillons de solution de concentrations connues. Elle reporte ensuite sur un graphe l’absorbance $A$ en fonction de la concentration $C$ et obtient alors la droite suivante appelée courbe d’étalonnage :
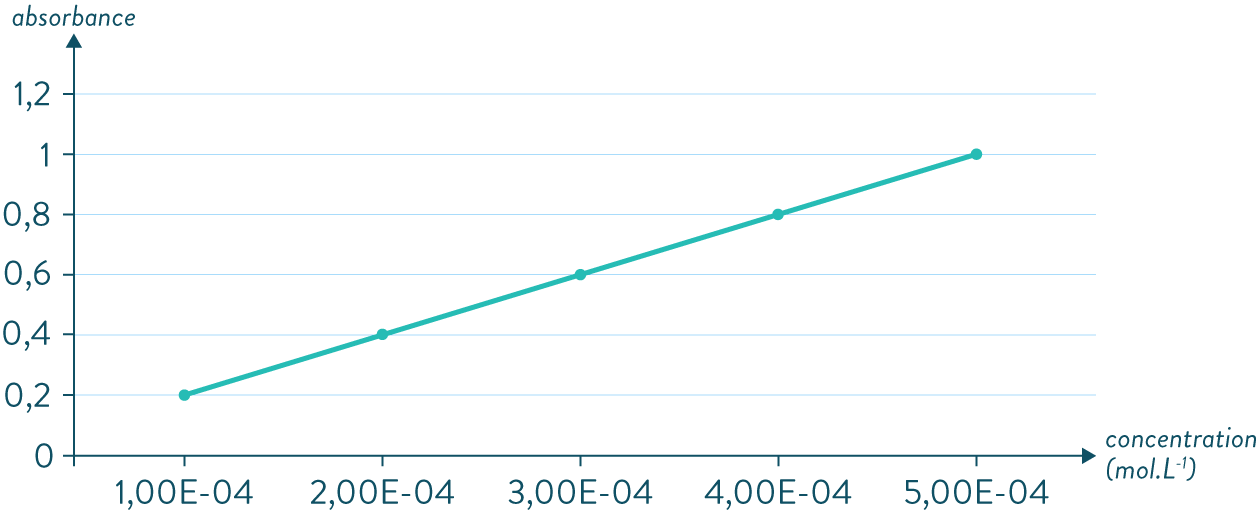 Courbe d’étalonnage du permanganate de potassium
Courbe d’étalonnage du permanganate de potassium
Concentration $(\text {mol} \cdot \text L^{-1})$ |
Absorbance |
$1,0 \times 10^{-4}$ |
$0,2$ |
$2,0\times 10^{-4}$ |
0,4 |
$3,0\times 10^{-4}$ |
$0,6$ |
$4,0 \times 10^{-4}$ |
$0,8$ |
$5,0 \times 10^{-4}$ |
$1$ |
L’équation de cette courbe d’étalonnage, déterminée expérimentalement, est donc :
$y=2,0 \times 10^3x$
De quelle méthode de dosage s’agit- il ? Ce dosage est-il perturbatif ?
Évaluation
Hélène veut vérifier que l’étiquette du vinaigre qu’elle vient d’acheter est conforme à sa teneur en acide acétique $(\text{CH}_3\text{COOH})$. Pour vérifier cela, elle commence par préparer une solution aqueuse de vinaigre diluée 50 fois appelée $S$. Ensuite $50\ \text{mL}$ de $S$ sont dosés par un titrage direct, suivi par pH-métrie, par une solution de soude $(\text{NaOH})$ de concentration $0,1\ \text{mol}\cdot \text{L}^{-1}$.
Elle note le $\text{pH}$ à chaque volume de soude rajouté et obtient la courbe de variation du $\text{pH}$ en fonction du volume de soude rajouté suivante
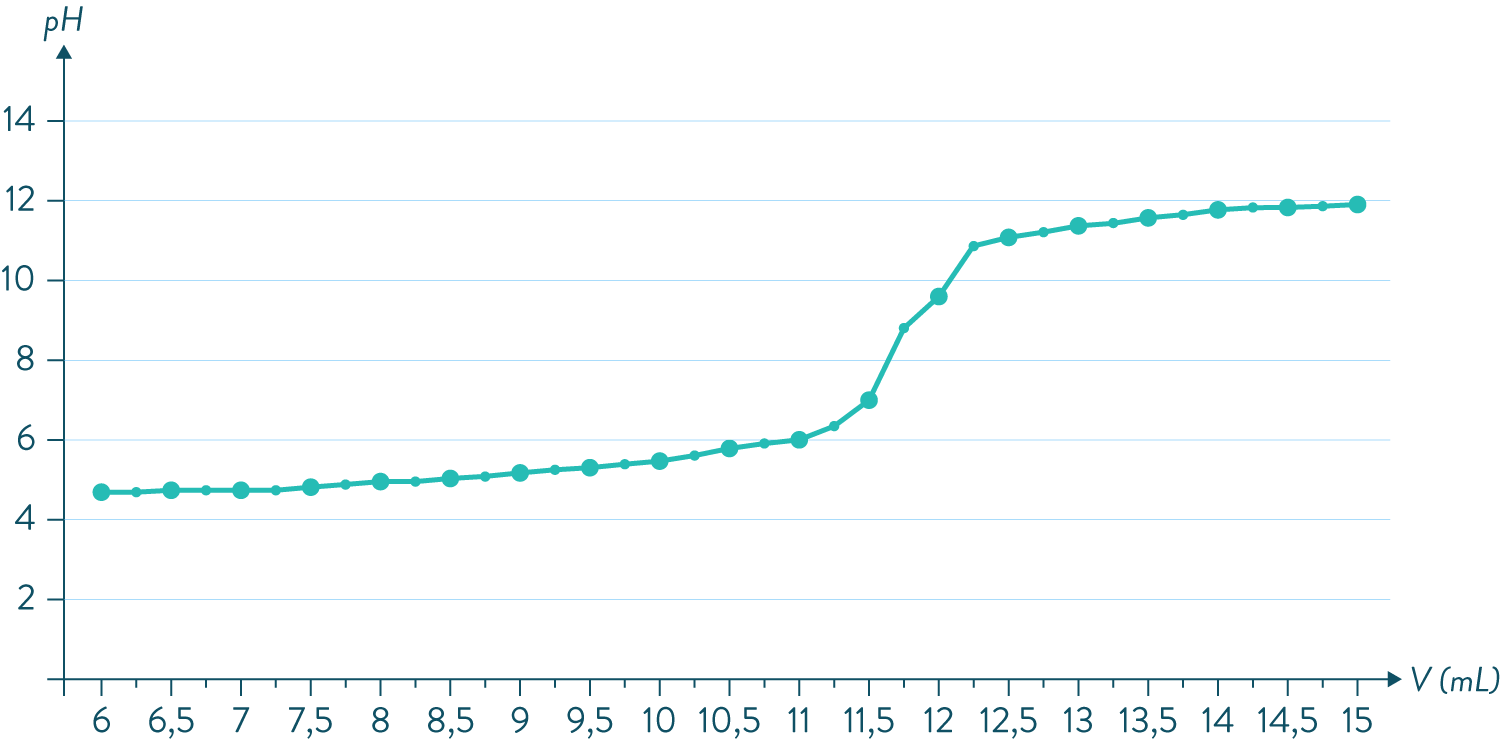 Variation du pH en fonction du volume de soude ajouté
Variation du pH en fonction du volume de soude ajouté
Données :
Les couples acide/base employés sont :
$\text{CH}_3\text{COOH}/\text{CH}_3\text{COO}^-$ et $\text H_2 \text O\text{OH}^-$
Quelles sont les caractéristiques d’une bonne réaction de support d’un dosage ?
